|
La Stabilizzazione del Neonato Critico |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
Mauro
Vivalda*, Paolo Gancia **
|
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
.
La stabilizzazione del neonato critico è il processo successivo alla rianimazione in sala parto ed è altrettanto fondamentale.Infatti rappresenta la prosecuzione dell’assistenza fornita al neonato al fine di consentirgli l’adattamento alla vita autonoma o, in caso di persistenza di condizioni critiche, la sopravvivenza in attesa del trasferimento in struttura idonea (TIN). La stabilizzazione, così come la rianimazione in SP, richiede cicli di valutazione, decisione ed azione orientati però a mantenere condizioni stabili nel tempo (sino al raggiungimento di attività autonoma o sino all’arrivo della equipe di trasporto - ricordiamo in questo caso che i tempi di attivazione + percorrenza medi sono di 60-90 minuti ). Occorre quindi prendere in considerazione i differenti aspetti della assistenza al neonato critico e prepararsi/attrezzarsi, per fornirla in modo continuativo per una/due ore. Per facilità mnemonica abbiamo coniato l’acronimo tre cime innevate che può aiutare a ricordare i vari aspetti che, in emergenza, devono essere esaminati e supportati: Termico. Respiratorio. Circolo. Metabolico. Infezioni. Neurologico. Vascolare. Terapia. Stabilizzazione termica Fisica della dispersione di calore Il neonato, soprattutto nei primi minuti dopo la nascita, disperde calore con facilità secondo tutte le modalità fisiche (evaporazione, conduzione, convezione, irraggiamento, etc.) Per questa ragione va posta grande attenzione nel limitare questo fenomeno: asciugare il piccolo ridurrà l’evaporazione e la convezione, porlo sotto una fonte di calore radiante o in unaculla termica ridurrà la conduzione, l’irraggiamento e, evitando spostamenti di aria,anche la convezione). Effetti della dispersione di calore La perdita di calore comporta, nel neonato,
Lo stress da freddo aumenta il rischio di ittero nucleare e aumenta la morbilità e la mortalità. . Dispositivi per evitare la dispersione di calore Incubatrice: in air-mode regolare a 33° C gradi per il nn a termine, → 37°C per il grande prematuro. In servo-controllata 36.3 → 36.9. Isola neonatale: accendere prima (sempre accesa in SP) per riscaldare il piano su cui si appoggia il nn., ricordare che aumenta l’evaporazione e che il nn. è esposto a correnti di aria (tenere sollevate le ali di protezione e muoversi con calma). Viene sconsigliato l’utilizzo di bottiglie o borse con acqua calda perché possono provocare ustioni. Condizioni termiche ideali in base all’EG
Temperatura corporea centrale ideale: 36,5-37,5°C Tabella dei valori termici di “benessere” in base al peso ed all’EG. * sconsigliato in caso di emergenza. . Stabilizzazione respiratoria Per attivare le procedure di stabilizzazione respiratoria del nn. occorre innanzitutto effettuare una corretta valutazione: questa passa attraverso la semeiotica classica per la diagnostica e l’impiego del punteggio di Silverman per la stadiazione del distress respiratorio. L’osservazione aiuterà, soprattutto i più esperti, nell’inquadramento del neonato che, a differenza del bambino e dell’adulto, rappresenta un “libro aperto” del quale è possibile sapere molto grazie alla semplice osservazione. Effettuata la rianimazione primaria, occorre valutare
* Alcuni strumenti rilevano la saturazione frazionale
(rapporto tra Hb ossigenata e Hb totale), altri lasaturazione funzionale,
cioè il
rapporto tra Hb ossigenata e Hb disponibile per il legame con l’O2:
dato che solo O2Hb e Hb ridotta (Hbr) hanno questo requisito, la
saturazione funzionale è uguale a O2Hb / (O2Hb + Hbr)
Per uniformare la terminologia impiegata per descrivere l’entità del distress respiratorio si propone la seguente classificazione(1):
. Score di Downes o RDS score – clinico
Score: ≥4 = distress respiratorio clinico; monitorare EGA ≥8 = Minaccia di insufficienza respiratoria . Emogasanalisi
Correlazione PaO2-SaO2
. . In base ai sintomi, si interverrà nell’assicurare
gli scambi gassosi servono sostanzialmente per
ossigenare il sangue e rimuovere la CO2; l’ossigenazione
dell’Hb è un dato rilevabile già alla
ispezione (anche se per ottenere un dato preciso
occorre come minimo la pulsossimetria). In tutte
le sale parto deve essere presente una fonte di ossigeno,
la cui somministrazione può avvenire: • flusso libero in incubatrice - in questo modo è possibile raggiungere percentuali del 30-50% - la % in O2 cala bruscamente ogni volta che si aprono gli oblò - è opportuno impiegare un ossimetro per avere un dato preciso (utile anche per prevedere la stabilità del nn. durante il trasporto) • flusso libero sotto cappa (Hood) - è possibile raggiungere elevate concentrazioni in O2, - non è molto comoda per i nn. “grossi”, - con bassi flussi di gas fresco, aumenta la percentuale di CO2 nell’aria inspirata • “occhialini” - con questo presidio si possono raggiungere elevate percentuali di O2, - è discretamente comodo anche per uso prolungato - ricordarsi di umidificare l’O2 → Ricordare che il neonato (il prematuro in particolare) è esposto ai danni da ossigeno e che il saturimetro fornisce un dato non sempre affidabile e soprattutto non fornisce il valore dalla PaO2 (cioè della tensione arteriosa in ossigeno). È possibile quindi che buoni valori disaturazioni corrispondano in realtà ad un’iperossia. Il consiglio è quello di mantenere valori di saturazione dell’Hb inferiori al 100%:nel prematuro l’obiettivo è una saturazione compresa tra 88 e 92%.
il supporto ventilatorio diviene necessario quando l’attività spontanea non sia sufficientemente valida, si avvale dell’uso di • mascherina - è uno strumento di uso immediato - può “sfiatare” se non viene mantenuta ben aderente al volto del bambino - può fare danni (se troppo grande: schiacciamento dei bulbi oculari.) • maschera laringea - impiego più facile rispetto al tubo endotracheale - diffusione ancora scarsa • tubo endotracheale - per la tecnica di intubazione si rinvia al manuale per l’emergenza in sala parto; - è necessario verificare il calibro del tubo in base al peso del nn. e la sua profondità di inserzione per evitare l’estubazione (poco probabile) oppure la ventilazione nel solo polmone dx per dislocazione troppo bassa del tubo (frequente) - è importante una buona tecnica di fissaggio del tubo (con 2 cerotti o con cerotto a H)
Per la ventilazione manuale si può impiegare: • Pallone tipo AMBU - Si possono raggiungere percentuali di O2 sino al 90% (con reservoir) - senza reservoir e con flusso di O2 di 5 l/min si eroga una miscela di gas con il 40 % di O2 - impiegando il pallone si possono raggiungere pressioni elevate (con rischio di PNX) soprattutto nel paziente intubato; ricordiamo la tecnica di 1 o più dita descritta nel manuale AHA-AAP(5) ma consigliamo di provare con l’ausilio di un manometro la propria sensibilità con lo strumento. - Nella ventilazione prolungata, occorre inoltre prestare attenzione alla frequenza degli atti respiratori imposti al nn. (FR) e del tempo in cui la pressione viene mantenuta, che corrisponde al tempoinspiratorio (Ti) Neo Puff - Con questo strumento sono impostabili le % O2 dal 21 al 100% (avendo a disposizione aria e O2) - le pressioni erogate sono controllate - occorre prestare attenzione a FR e Ti La ventilazione meccanica del neonato è generalmente praticata con ventilatori a limite di pressione e ciclo di tempo. Parametri standard:
Dopo aver assicurato un’adeguata ventilazione, e solo dopo questa fase, ci si preoccuperà di avere una diagnosi eziologica del distress e di rimuovere, quando possibile, la causa. Tabelle. Calibro del tubo endotracheale in base al peso ed all’età gestazionale (AHA–AAP(5)) Profondità di inserzione del tubo endotracheale in base al peso (AHA–AAP(5))
profondità di inserzione = 6 + peso in kg del neonato + 1 cm
se intubato dal naso ( 2 cm se > 2 kg) Clinicamente: Il margine superiore del marcatore nero sulla punta del tubo ET dovrebbe essere posizionato a livello delle corde vocali: tenere presente che può avere lunghezza diversa a seconda del calibro del tubo e delle ditte produttrici. Radiograficamente: Posizione ideale:punta a livello del corpo di T1 Posizione accettabile: in un punto compreso tra l’estremità mediale della clavicola e 1,5 cm al disopra della carena Stima rapida della profondità di inserzione: Lunghezza naso-trago (NTL): dalla radice del setto nasale al trago Lunghezzadello sterno (STL): dall’incisura soprasternale all’apice del processo xifoideo Intubazione orotracheale: NTL (o STL) + 1 cm Intubazione nasotracheale: NTL (o STL) + 2 cm Cannello per O2
Cella (Hood) . . Occhialini . Incubatrice
Ossimetro . Maschera/pallone . . Intubato/pallone . . Neo puff . La sedazione del neonato In caso di intubazione particolarmente difficoltosa per la reattività del paziente si potrà prendere in considerazione la sedazione farmacologica. Nel nostro centro impieghiamo boli di midazolam 0,05 mg/kg/dose eventualmente ripetuti (fiala 1 ml: 5 mg, diluire a 10 e di nuovo a 10, dose: 1 ml/kg). → Avvertenza: Il midazolam può dare ipotensione. Surfactant esogeno Il surfactant esogeno è efficace nelle patologie da carenza (malattia delle membrane ialine) ma, come tutti i farmaci ha importanti effetti collaterali: - migliora rapidamente la compliance polmonare e la ventilazione alveolare, e quindi richiede un parallelo adeguamento dell’assistenza ventilatoria: questa è più efficace se il paziente è adeguatamente monitorato e se si impiega un ventilatore meccanico sincronizzato (il ventilatore dell’incubatrice da trasporto non possiede tali requisiti), - migliora gli scambi gassosi, con possibile ipocapnia (e quindi vasocostrizione cerebrale) ed iperossia, - inoltre la somministrazione stessa non è esente da possibili incidenti (ad esempio l’irrigazione di un solo polmone per dislocazione del sondino troppo in basso). Per queste ragioni non si ritiene opportuno l’impiego di surfactant nei centri invianti. Pneumotorace Il pneumotorace è un evento critico non infrequente in un neonato soprattutto se sottoposto a rianimazione. - prevenzione del PNX traumatico: può essere fatta
- presidio fondamentale della diagnosi è il sospettare un PNX in un nn.
- Diagnosi clinica:
» la t. si esegue con una sorgente di luce fredda » dopo aver creato il buio nel locale si posiziona la lampada sul torace e si osserva attraverso la trasparenza della parete l’eventuale presenza di aria libera (in caso di pnx si illumina non solo l’area immediatamente circostante la fonte luminosa ma anche parte o tutto l’emitorace) » in alcuni casi la t. è l’unico strumento diagnostico impiegabile per ragioni logistiche o di tempo; in caso di estrema necessità può confortare il sospetto clinico, permettendo un decompressione immediata.
» Il quadro radiografico di un PNX è caratterizzato da ipertrasparenza dell’emitorace contenente aria libera, la trama polmonare non è visualizzabile se non in regione ilare (zona dove collassa il polmone), se il pnx è iperteso si può avere spostamento del mediastino e compressione del polmone controlaterale. » Attenzione alle false immagini (plica cutanea o del telino che si continua sotto il diaframma, parenchima presente esternamente alla plica) La decompressione in emergenza del PNX In caso di PNX iperteso con sintomatologia clinica ingravescente (scambi gassosi inefficaci nonostante ventilazione e O2 , bradicardia ..) deve essere rapidamente effettuata la decompressione. Si consiglia l’impiego di
La procedura prevede
Transilluminazione di un PNX
. Drenaggio PNX (set posizionato per aspirazione/espulsione aria libera)
Stabilizzazione
del circolo Lo shock in epoca neonatale può essere: • ipovolemico: è la forma più frequente, generalmente legata a - perdita di sangue per distacco di placenta, - clinicamente il neonato si presenta IPOTESO, con VASOCOSTRIZIONE PERIFERICA, CIANOSI PALLIDA, ACIDOSI. - La diagnosi si avvale, oltre la semeiotica classica, della rilevazione della pressione sanguigna e della valutazione del tempo di ricolorazione: si esegue applicando con il pollice per 5” la minima pressione in grado di far impallidire la cute, preferibilmente sul punto medio dello sterno o sulla frontee misurando il tempo necessario per il riempimento capillare. - La bassa temperatura ambientale e cutanea riduce il flusso ematico e prolunga il TRC. I pannelli radianti, l’incubatrice ela fototerapia possono invece aumentare il flusso ematico locale. - Il limite superiore di normalità è pari a 3”, indipendentemente dall’EG e dal peso. - La terapia prevede il ripristino delle perdite con soluzioni elettrolitiche, plasma o sangue. In pratica, considerata la difficoltà nell’ottenere derivati ematici in tempi brevi, si consiglia l’impiego, in emergenza, di soluzione fisiologica 10-20 ml/kg in infusione rapida (in 10-20 minuti o addirittura a bolo in base alle condizioni cliniche) • cardiogeno Il nn. può manifestare insufficienza cardiaca in seguito ad - Asfissia - Ipossia - Ipoglicemia severa - Infezioni - Cardiopatie congenite/aritmia prolungata Le manifestazioni cliniche saranno ALTERAZIONE DEL CIRCOLO PERIFERICO, DELLA FC (tachicardia), RESPIRATORIE, PRESSORIE La terapia prevede l’infusione di espansori di volume, l’impiego di farmaci inotropi (amine) e la correzione dell’acidosi: soluzione fisiologica 10-20 ml/kg, dopamina a 10 mcg/kg/min, sodio bicarbonato diluito 1:1 → 4 ml/kg a bolo lento • settico - Il neonato infetto può andare incontro a shock per vasodilatazione, stravaso di liquidi al di fuori dello spazio vascolare, depressione miocardica. - Le manifestazioni cliniche saranno dunque l’insieme di quelle presentate nello shock ipovolemico e da quello cardiogeno. - La terapia prevede l’infusione di espansori di volume, l’impiego di farmaci inotropi (amine) e la correzione dell’acidosi: soluzione fisiologica 10-20 ml/kg, dopamina a 10 mcg/kg/min, sodio bicarbonato diluito 1:1→ 4 ml/kg a bolo lento - Possono inoltre essere impiegati steroidi e.v. Flebocortid 20-50 mg/kg/dose Tabella diluizioni dopamina
Pressioni arteriose accettabili (13)
. Stabilizzazione metabolica L’ipoglicemia Neonati a rischio di ipoglicemia debbono essere considerati tutti i quelli che abbiano avuto un evento patologico e non possano essere adeguatamente alimentati per os, oltre a tutti i prematuri ed agli SGA. → Fornire glucosio endovena e determinare i valori glicemici di ogni neonato di cui si richiedeil trasporto. Valori normali: sonocontroversi i valori accettabili di glicemia per i neonati. La soglia di glicemia “sicura” per eventi acuti come il coma e le convulsioni è di 20 mg/dl per i nati pretermine e di 30 mg/dl nei nati a termine. Sono state rilevate alterazioni cerebrali documentate in RMN nella grave ipoglicemia protratta. Inoltre gli studi di Lucas(2) hanno dimostrato che nel prematuro l’esposizione a valori glicemici <45 mg/dl per periodi prolungati (ore), anche non consecutivi, si associano a ridotte prestazioni intellettive a sviluppo neurologico completato. Per questa ragione si propone di non tollerare glicemie < 45 mg/dl, indipendentemente dall’età gestazionale. Metodi diagnostici. La determinazione della glicemia può essere effettuata con: • metodi rapidi (es. glucotrend – destrostix) . - Occorre però tenere presente che essendo metodiche sviluppate per l’adulto diabetico (e quindi per essere precise per valori tra i 100 ed i 300 mg/dl), non sono molto precise per la determinazione dei valori che interessano il Neonatologo. • Metodiche di laboratorio - In questo caso l’affidabilità è buona purché il campione venga esaminato immediatamente dopo il prelievo dal momento che nel sangue in provetta continua il consumo di glucosio. - Gli emogasanalizzatori di recente
generazione sono in grado di determinare i valori
glicemici con metodiche affidabili. Calcolo del fabbisogno in glucosio: dovendo trattare preventivamente un neonato a rischio di ipoglicemia, si calcola un fabbisogno in glucosio di 4-6 mg/kg/min. In caso di ipoglicemia conclamata il fabbisogno potrà essere più elevato (sino a 8 mg/kg/min e oltre). Calcolo dei liquidi: dal momento che il glucosio viene somministrato in soluzione acquosa e che non è bene superare una concentrazione del 10-12% se non si impiega un accesso vascolare centrale, si deve tenere conto di questi vincoli per evitare la somministrazione di adeguate quantità di glucosio coneccessive quantità di liquidi. Il fabbisogno di liquidi di un neonato varia dai 60 ai 120 ml/kg a seconda delle condizioni e dell’età gestazionale.Un eccessivo apporto di liquidi può essere dannoso (soprattutto in pazienti con distress respiratorio con edema polmonare). In genere è possibile far corrispondere la quantità di glucosio con il fabbisogno idrico del neonato: 3 ml/kg/ora (ovvero 72 ml/kg/die) di soluzione glucosata al 10% corrispondono a circa 5 mg/kg/min. di glucosio. Con circa 5 ml/kg/ora (120 ml/kg/die) si raggiungono gli 8 mg/kg/min. In caso di ipoglicemia severa è consigliabile correggere la glicemia lasciando in secondo luogo il problema idratazione. → quando la somministrazione di glucosio supera gli 8 mg/kg/min. è indicato ricorrere agli steroidi endovena ed al glucagone. Soluzione glucosata 10% → 3 ml/kg/oraper fornire Glucosio → 5 mg/kg/min L’acidosi In fase acuta il neonato critico manifesta generalmente un quadro di acidosi mista; infatti l’asfissia perinatale comporta una condizione di acidosi metabolica, mentre l’insufficienza respiratoria determina acidosi respiratoria. La correzione dell’acidosi respiratoria è sempre prioritaria e, quasi sempre, risolutiva. Infatti migliorando la ventilazione si facilita la rimozione dell’anidride carbonica abbassando il rapporto CO2/HCO3 a favore dei bicarbonato. Riducendo la componente respiratoria dell’acidosi si compensa la componente metabolica; quest’ultima, rimosse le cause, scompare di conseguenza. Dal momento che la rimozione della CO2 è principalmente dovuta alla frequenza respiratoria, la ventilazione di un paziente in acidosi, dovrà essere a frequenza elevata (40-60 atti o più). L’impiego di alcalinizzanti per via sistemica è raro e viene riservato al caso di acidosi metabolica persistente nonostante l’adeguata rimozione della CO2 (in linea di massima eccesso di basi negativo ≤10 che persista oltre le 2-3 ore dall’inizio di una ventilazione efficace). Si utilizza il sodio-bicarbonato alla dose di 2 mEq/kg pro dose iniettato lentamente, ripetibile. NaHCO3: 2 mEq/kg/dose (fiale 1 mEq/ml diluito 1:1 con acqua distillata → 4 ml/kg/dose)
Le infezioni neonatali Il neonato a rischio infettivo Deve essere considerato a rischio per infezioni il neonato che presenti i seguenti fattori pre-perinatali o che sia stato sottoposto a manovre invasive: • Fattori pre-perinatali: - Corioamniotite, - Febbre materna, - PROM, - Prematurità - TV positivo per SGB, • Manovre invasive - Intubazione - CVO - altro E’ universalmente riconosciuta l’utilità della profilassi antibiotica in caso di rischio infettivo in neonato sintomatico. Il neonato, infatti, a differenza del bambino o dell’adulto, è un paziente immunodepresso in cui una infezione, anche da germi non molto aggressivi, può divenire rapidamente una sepsi che, altrettanto rapidamente può determinare una situazione di shock e portare all’exitus. Per queste ragioni, in caso di rischio reale, è preferibile mantenere un atteggiamento “aggressivo” impiegando una penicillina in associazione ad un aminoglicoside a dosaggio pieno. La scelta dei farmaci da impiegare deve infatti considerare i possibili germi in causa e fornire una copertura ad ampio spettro. I farmaci che vengono impiegati nel nostro Repartosono: Ampicillina 50 mg/kg + Gentamicina 5 mg/kg E’ bene far precedere alla somministrazione dei farmaci un prelievo per emocoltura (che sarà utile per documentare l’infezione, fornire dati statistici sul tipo di germi coinvolti nella nostra realtà, e guidare tramite antibiogramma la successiva terapia). Sepsi neonatale La sepsi neonatale viene spesso,
nelle prime fasi, solo sospettata: l’espressione clinica è,
inizialmente, simile a molte altre patologie acute dell’età neonatale
(di stress respiratorio, alterazioni del circolo, ipotonia,
iporeattività, letargia); gli esami laboratoristici
sono spesso di scarso o nessun aiuto (la leucocitosi non
sempre è presente, quando invece si è giunti
alla leucopenia è ormai troppo tardi; la PCR non
muove abbastanza rapidamente e la sua produzione è dipendente
dalla risposta leucocitaria del nn: se il nn non risponde
con leucocitosi va incontro ad una sepsi gravissima senza
far aumentare la PCR) anche la radiodiagnostica aiuta poco:
il quadro iniziale di polmonite da SGB è indistinguibile
da quello dell’RDS. Per queste ragioni si consiglia di iniziare presto una terapia aggressiva se vi è il fondato sospetto (o anche solo il ragionevole dubbio). In caso di sepsi conclamata si praticheranno inoltre le terapie di supporto del caso: - assistenza ventilatoria per il distress respiratorio - accesso venoso per la correzione di Ipoglicemia/acidosi - presidi terapeutici anti-Shock Aspetti neurologici La valutazione dell’aspetto neurologico del neonato può fornire elementi utili al processo decisione/azione, contribuire alla formulazione di una prognosi e, in alcuni casi, indurre alla scelta di un approccio terapeutico preciso: l’ipotermia cerebrale, che deve essere applicata entro tempi ben definiti e nella struttura idonea. Da un punto di vista pratico possiamo distinguere, in base all’età gestazionale, due categorie di neonati: il neonato pretermine (in particolare se inferiore alle 34 sett.) ed il neonato a termine. Il neonato pretermine - è frequentemente depresso in modo aspecifico e spesso tale sintomatologia non si associa ad esiti patologici; - è fondamentale, per lui, la terapia di supporto, considerata la scarsa capacità di adattamento e la maggiore suscettibilità allo stress di qualunque natura; - occorre prestare molta attenzione al controllo degli scambi gassosi: » sono descritti danni da iperossia oltre a quelli già noti dell’anossia, » l’ipercapnia e l’ipocapnia sono entrambe dannose (peggiore comunque la condizione di ipocapnia per la quale è documentata l’associazione a leucomalacia periventricolare); - l’ipotensione ed in generale da disturbi del circolo, possono crearedanni, in particolare è ben noto il danno cerebrale da associazione ipotensione-ipossiemia; - l’ipoglicemia è un’altra causa di danno acuto/permanente del SNC del neonato pretermine. → si consiglia un approccio deciso ma improntato ad una correzione “lenta” delle condizioni di patologia del neonato pretermine: spesso è infatti più dannoso il rapido ripristino di una condizione ottimale della stessa permanenza nella situazione di scompenso preesistente. → ventilare con miscele di aria e ossigeno (l’iperossia è dannosa) → tenere saturazione di 02 tra 88-92 (il feto fino a poco prima in utero aveva saturazioni tra 30 e 40%) → tenere la PC02 non >55mmHg (rischio di emorragia cerebrale) e non inferiore a 30mmHg (rischio di ischemia) → prestare molta attenzione ad evitare l’associazione ipossia, ipotensione ed ipoglicemia perché l’effetto di danno cerebrale è sinergico. Il neonato a termine Il nn. a termine può presentarsi depresso in risposta a condizioni patologiche in cui si sia trovato prima, durante o dopo la nascita: per stato settico, per malattia metabolica e spesso per condizioni non chiaramente identificabili in fase di stabilizzazione. La valutazione clinica può essere più precisa impiegando icriteri di Sarnat e Sarnat (inoltre l’inquadramento in stadi consente di formulare una prognosi in base alla gravità). In base alla pratica comune si possono effettuare le seguenti considerazioni: - la presenza di sofferenza fetale acuta (alterazioni del BCF, liquido tinto..) pone il nn. a rischio di asfissia e quindi di danno neurologico; - l’apnea alla nascita conferma questo rischio; occorre tenere presente che il tempo necessario all’instaurarsi di una attività respiratoria valida è direttamente proporzionale alla durata dell’asfissia; - l’attività cardiaca è l’ultima a cedere per cui l’asistolia è un sintomo di estrema gravità ed il perdurare di asistolia oltre i 10-15’ di rianimazione efficiente si associa ad esiti neurologici gravissimi qualora il neonato sopravviva; - la depressione neurologica (risposta letargica o comatosa agli stimoli dolorifici) e/o le convulsioni esprimono la presenza di un danno (non necessariamente permanente) del SNC; - l’indice di APGAR al 5’ fornisce una affidabile indicazione circa il grado di sofferenza cerebrale: è probabileche un nn. con APGAR al 5’ <5 vada incontro a patologia neurologica acuta o cronica. - un altro indicatore è l’entità della acidosi metabolica rilevata con EGA arterioso entro 1 ora di vita: un pH=7.1, e/o un BE-10 vengono considerati i limiti. → Nel nostro centro i neonati che siano andati incontro ad asfissia perinatale con segni di sofferenza fetale ed abbiano APGAR<5 al 5’ + pH<7.1 e/o Be<-10 + sintomatologia neurologica (letargia/convulsioni) vengono posti in IPOTERMIA entro 6 ore dalla nascita nel tentativo di ridurre il danno cellulare secondarioe quindi gli esiti a distanza. Per questa ragione si consiglia ai centri afferenti al nostro servizio di attivare con rapidità il trasporto neonatale qualora il neonato sia nelle condizioni sopra descritte (o sia ipotizzabile che le sviluppi nelle ore successive alla nascita). Per uniformare la terminologia impiegata per descrivere la sintomatologia neurologica si propone la seguente classificazione (1): reattivo (reattivo agli stimoli dolorosi, pianto vigoroso) letargico (torpida risposta agli stimoli dolorosi, pianto flebile) coma (assente risposta agli stimoli dolorosi, convulsioni, atonia) La terapia delle convulsioni è classicamente basata sull’impiego dei barbiturici e, in seconda battuta, in urgenza, delle benzodiazepine: Fenobarbitale 20 mg/kg +10 mg/kg + 10 mg/kg Diazepam 0,2 mg/kg/dose ripetibile Saranno praticate inoltre le terapie di supporto del caso: spesso si associa:
Stadiazione di Sarnat e Sarnat
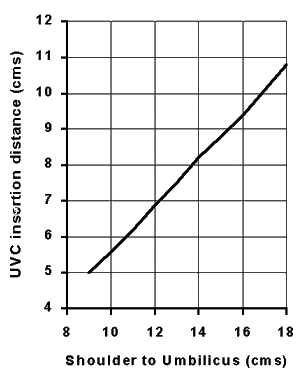
L’accesso vascolare nel neonato Il neonato patologico che richiede trasporto dovrà avere un accesso vascolare (per l’infusione di soluzioni glucosate o per la somministrazione di farmaci). Ricordando che la somministrazione di farmaci in urgenza è possibile, se non probabile, e che non sempre è facile procurarsi un accesso in urgenza, è imperativo posizionare un accesso appena possibile e non trasportare un paziente privo di un accesso vascolare sicuro. Accesso venoso periferico: - si ricorda la difficoltà nell’infondere grandi volumi e liquidi ad elevata osmolarità (SG a concentrazione non oltre il 12,5%); - si propone, se possibile, di risparmiare i vasi della piega del gomito ed ascellari, che vorremmo riservare alla successiva introduzione di CVC percutaneo. Accesso venoso centrale: la vena ombelicale è vaso di facile accesso e di grande portata per cui viene abitualmente incannulata in emergenza. Devono essere tenute presenti le seguenti considerazioni: - durante la recisione del moncone ombelicale si può avere sanguinamento (per evitare questo problema si consiglia di recidere a 1-2 cm dal piano cutaneo avendo preventivamente posizionato un nodo scorsoio alla base del M.O. tale da poter essere chiuso con rapidità, se necessario); - emorragia si può avere anche in un secondo tempo (per il miglioramento delle pressioni del nn. o per la dislocazione del catetere) si consiglia quindi di porre attenzione all’emostasi (il modo più semplice è quello di chiudere definitivamente il nodo scorsoio di cui sopra – la manovra impedirà però il successivo posizionamento di catetere arterioso ombelicale per cui è conveniente concordare le modalità difissaggio con gli operatori del nostro centro) e di fissare accuratamente il CVO in modo che non possa sfilarsi (con filo per sutura o con cerotti). - Il posizionamento dell’estremità distale del CVO in emergenza (senza un riscontro radiografico o ecografico) non può essere considerato sicuro: nel suo percorso, prima di superare il dotto di Aranzio, incontra infatti i vasi epatici in cui potrebbe incunearsi; inoltre, superata la vena cava inferiore può entrare nelle cavità cardiache e provocare traumatismo di parete per ragioni meccaniche o osmolari. Si consiglia pertanto il posizionamento “basso” a 2-3 cm dal piano cutaneo, ricordando che una quota delle soluzioni infuse andrà direttamente al fegato (dunque non è consigliabile l’infusione di amine, Ca Gluconato, soluzioni iperosmolari, se non in caso di assoluta emergenza). - qualora sia possibile il posizionamento del CVO in modo definitivo, si allegano le tabelle utili per conoscere approssimativamente la profondità di inserzione:la certezza si ha solo con l’ausilio della diagnostica strumentale. Tabella posizione CVO La terapia farmacologica I farmaci di comune impiego in emergenza neonatale sono i seguenti: • in infusione continua: DOPAMINA 1 ml = 40 mg ..................10mcg/kg/min DOBUTAMINA 1 ml = 12,5 mg......... 10mcg/kg/min ALPROSTADIL 1ml = 0,5 mg ............0,05mcg/kg/min MIDAZOLAM 1 ml = 5 mg ................0,5 mcg/kg/min • a bolo: MIDAZOLAM 1 ml = 5 mg ................0.05 mg/kg/dose LORAZEPAM 1 ml = 4 mg .................0,05 mg/kg/dose FUROSEMIDE 2 ml = 20 mg..............1-2 mg/kg/dose Na bicarbonato 1 ml = 1 mEq ..............2 mEq (4 ml)/kg/dose ADENOSINA 2 ml = 6 mg...................0,1 mg/kg LIDOCAINA.1 ml = 20 mg..................1 mg/kg FENOBARBITALE 1 ml = 30 mg.......20 mg/kg/dose + 10 mg/kg + 10 mg/kg
Patologia Cardiaca In generale la patologia cardiaca acuta in epoca neonatale è dovuta a cardiopatie congenite. Meno frequentemente possono aversi problemi legati ad aritmie. Cardiopatie congenite • cardiopatie cianogene - il problema è la ipossiemia resistente all’ossigeno, che richiede trattamento cardiochirurgico in tempi brevi, - si tratta di patologie cardiache in cui la cianosi è causata dal mescolamento di sangue venoso attraverso uno shunt dx->sx su base malformativa - il sospetto diagnostico viene confermato mediante test di iperossia - l’ecocardiografiaconsente la diagnosi definitiva - è importante porre diagnosi (o per lo meno il fondato sospetto) già in sede periferica per indirizzare il trasporto verso un centro cardiochirurgico - la stabilizzazione prevede la somministrazione » di ossigeno e l’eventuale supporto ventilatorio (evitando l’ipocapnia) » e, se non è possibile ottenere saturazioni dell’Hb>80%, di prostaglandine in infusione continua alprostadil 0,05-0,1 mcg/kg/min • cardiopatie con scompenso - il problema è lo scompenso cardiaco congestizio che si instaura progressivamente, generalmente in alcuni giorni ma in certi casi anche in tempi più brevi, ed è negativamente condizionato dalla chiusura del dotto arterioso, - sono in genere dovute alla necessità, da parte del muscolo cardiaco, di pompare contro pressioni aumentate o con aumentati volumi di sangue (per ricircolo attraverso comunicazioni intracardiache), - la stabilizzazione prevede l’impiego di diuretici furosemide 2 mg/kg/dose di prostaglandine in infusione continua alprostadil 0,05-0,1 mcg/kg/min oltre all’eventuale supporto ventilatorio
Il paziente chirurgico Gastroenterico Atresia esofagea/fistola tracheo-esofagea - la diagnosi, solitamente ecografica in utero (polidramnios – impossibilità della visualizzazione dello stomaco) impone il trasferimento in utero a centro dotato di chirurgia neonatale, - in caso manchi l’accertamento ecografico, il sospetto si pone in un neonato che manifesti scialorrea associata o meno a distress respiratorio, soprattutto se in concomitanza all’assunzione di latte. -la diagnosi si conferma introducendo un sondino attraverso l’esofago: in caso di atresia lo stesso non procede. Non è indispensabile effettuare subito la diagnostica dell’eventuale fistola associata - se il nn. manifesta dispnea occorrerà aspirare il contenuto della sacca esofagea ed assistere la ventilazione in base all’entità della sintomatologia. * il tubo endotracheale può ostruire la fistola eliminando temporaneamente il problema, mentre la ventilazione in maschera può aumentare la distensione gastrica in caso di fistola distale. - il nn. deve essere posto in aspirazione continua (a bassa pressione) o, se si opta per la aspirazione manuale, aspirato frequentemente (almeno ogni 15 min). - viene inoltre consigliata la posizione obliqua a 45° per ridurre il reflusso -non essendo possibile l’alimentazione enterale è indispensabile posizionare un accesso venoso per garantire l’apporto di liquidi Ernia diaframmatica - Come per l’atresia esofagea, la diagnosi è generalmente prenatale, anche se è possibile il caso di erniazione dei visceri alla nascita. -Il sospetto si pone in nn. con distress respiratorio, respiro ipotrasmesso in un emitorace, battito cardiaco spostato, addome piatto (o addirittura scafoide); la diagnosi è radiografica; -Questi soggetti vanno intubati d routine, poiché la ventilazione in maschera peggiora la distensione dello stomaco e del piccolo intestino, e quindi la compressione sul polmone; - È frequente lo sviluppo di pneumotorace a causa dei gasping durante la rianimazione primaria, dell’opposizione al ventilatore o di picchi di pressione inappropriati. - È necessario posizionare un sondino gastrico in aspirazione per decomprimere lo stomaco e il piccolo intestino - Anche in questo caso, non essendo possibile l’alimentazione entrale, è indispensabile posizionare un accesso venoso per garantire l’apporto di liquidi. Onfalocele/gastroschisi - sono entrambe patologie con fuoruscita dei visceri addominali, in genere diagnosticate in utero e dunque trasferite in utero; - l’assistenza si indirizza alla protezione (con garze sterili inumidite con soluzione fisiologica) ed alla prevenzione della disidratazione conseguente alla rapida evaporazione del liquido contenuto nei visceri erniati. - Anche in questo caso non essendo possibile l’alimentazione enterale è indispensabile posizionare un accesso venoso per garantire l’apporto di liquidi.
Il paziente neurologico Difetti del tubo neurale: Mielo/Meningocele - l’assistenza si indirizza alla protezione (con garze sterili inumidite con soluzione fisiologica appoggiate su garze antiaderenti) ed alla prevenzione delle infezioni (copertura antibiotica ad ampio spettro), in attesa del trasferimento in Neurochirurgia.
Bibliografia
Gli autori ringraziano per la collaborazione prestata nell’ambito dei Corsi di Stabilizzazione del Neonato Critico: I Dirigenti Medici della SC TIN – Neonatologia, ASO S. Croce e Carle, Cuneo Dr. Raffaele Basta Dr. Antonio Delogu Dr. Stefano Gabrielli Dr. Giulia Pomero La Caposala AFD Giuliana Cavallero L’équipe infermieristica della SC TIN – Neonatologia
.
. |
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||